Обсуждение:Работа с газами: различия между версиями
м MiHaNiK849 переименовал страницу Обсуждение:Смешивание газов в Обсуждение:Работа с газами: Название с ошибкой |
Нет описания правки |
||
| (не показана 1 промежуточная версия 1 участника) | |||
| Строка 5: | Строка 5: | ||
|info = | |info = | ||
}} | }} | ||
{{ | {{Guide|ENG}} | ||
<br> | <br> | ||
<br> | <br> | ||
| Строка 14: | Строка 14: | ||
{{quote|Что такое фрезон и с чем его дышат?}} | {{quote|Что такое фрезон и с чем его дышат?}} | ||
<h2 style="border-bottom:2px solid #{{ColorPalette| | <h2 style="border-bottom:2px solid #{{ColorPalette|Atmospheric|Primary Bold}}>Газы</h2> | ||
Тут описаны свойства газов которые есть в SS14 на данный момент | Тут описаны свойства газов которые есть в SS14 на данный момент | ||
{| class="wikitable sortable" style="width:100%" | {| class="wikitable sortable" style="width:100%" | ||
| Строка 23: | Строка 23: | ||
! style="border-bottom:1px solid gold"| Молярная масса (г/моль) | ! style="border-bottom:1px solid gold"| Молярная масса (г/моль) | ||
! style="border-bottom:1px solid gold"| Цена за Моль (Кредиты) | ! style="border-bottom:1px solid gold"| Цена за Моль (Кредиты) | ||
! style="border-bottom:1px solid gold"| Конденсируется | |||
|- | |- | ||
! | ! {{Gas|Oxygen|}}<br>Кислород | ||
| Бесцветный газ без запаха. Люди должны дышать, чтобы оставаться в живых. Окислитель в большинстве реакций горения. | | Бесцветный газ без запаха. Люди должны дышать, чтобы оставаться в живых. Окислитель в большинстве реакций горения. | ||
| 20 | | 20 | ||
| 32 | | 32 | ||
| 0 | | 0 | ||
| [[Химия#chem_Oxygen | Кислород]] | |||
|- | |- | ||
! | ! {{Gas|Nitrogen}}<br>Азот | ||
| Бесцветный газ без запаха. Сам по себе безопасен при вдыхании человеком. Необходим бля дыхания слаймолюдам. | | Бесцветный газ без запаха. Сам по себе безопасен при вдыхании человеком. Необходим бля дыхания слаймолюдам и воксам. | ||
| 30 | | 30 | ||
| 28 | | 28 | ||
| 0 | | 0 | ||
| [[Химия#chem_Nitrogen | Азот]] | |||
|- | |- | ||
! | ! {{Gas|CarbonDioxide}}<br>Углекислый газ | ||
| Бесцветный газ без запаха. Выдыхается существами, дышащими кислородом. При высокой концентрации он становится токсичным для всех кроме дион. | | Бесцветный газ без запаха. Выдыхается существами, дышащими кислородом. При высокой концентрации он становится токсичным для всех кроме дион. | ||
| 30 | | 30 | ||
| 44 | | 44 | ||
| 0 | | 0 | ||
| [[Химия#chem_CarbonDioxide | Диоксид углерода]] | |||
|- | |- | ||
! | ! {{Gas|NitrousOxide}}<br>Оксид азота | ||
| Бесцветный газ без запаха. Также известный как «веселящий» или «сонный» газ, он действует как успокаивающее средство на всех, кроме слизней, и токсичен в очень высоких концентрациях. Это вещество выдыхается слизнями. | | Бесцветный газ без запаха. Также известный как «веселящий» или «сонный» газ, он действует как успокаивающее средство на всех, кроме слизней, и токсичен в очень высоких концентрациях. Это вещество выдыхается слизнями. | ||
| 40 | | 40 | ||
| 44 | | 44 | ||
| 1 | | 1 | ||
| - | |||
|- | |- | ||
! | ! <center>{{Gas|Plasma}}</center><br>Плазма | ||
| Розово-фиолетовый, легковоспламеняющийся, ядовитый газ. В присутствии кислорода загорается при воспламенители или температуре выше 100 °С. Этот газ жизненно важен для производственной и научной деятельности на борту станции. | | Розово-фиолетовый, легковоспламеняющийся, ядовитый газ. В присутствии кислорода загорается при воспламенители или температуре выше 100 °С. Этот газ жизненно важен для производственной и научной деятельности на борту станции. | ||
| 200 | | 200 | ||
| 120 | | 120 | ||
| 0 | | 0 | ||
| [[Химия#chem_Plasma | Плазма]] | |||
|- | |- | ||
! | ! <center>{{Gas|WaterVapor}}</center><br>Водяной пар | ||
| Выглядит как белое облако, вода в газообразном состоянии. Не конденсируется в жидкую воду. Вреден для слаймолюдов. | | Выглядит как белое облако, вода в газообразном состоянии. Не конденсируется в жидкую воду. Вреден для слаймолюдов. | ||
| 40 | | 40 | ||
| 18 | | 18 | ||
| 0 | | 0 | ||
| [[Химия#chem_Water | Вода]] | |||
|- | |- | ||
! | ! <center>{{Gas|Miasma}}</center><br>Миазмы (Аммиак) | ||
| Тёмно-фиолетовый, зловонный газ. Ядовит и вреден в достаточно больших концентрациях. Побочный продукт неприятных биологических процессов, например, гниения тел. Может выделятся крысиным королём. | | Тёмно-фиолетовый, зловонный газ. Ядовит и вреден в достаточно больших концентрациях. Побочный продукт неприятных биологических процессов, например, гниения тел. Может выделятся крысиным королём. | ||
| 20 | | 20 | ||
| 44 | | 44 | ||
| 0.15 | | 0.15 | ||
| [[Химия#chem_Ammonia | Аммиак]] | |||
|- | |- | ||
! | ! <center>{{Gas|Tritium}}</center><br>Тритий | ||
| Зеленый, легковоспламеняющийся и [[Врач#Отравление, радиация и другие вредные частицы|радиоактивный]] при вдыхании газ. Горит в присутствии кислорода. Получается как побочный продукт при горении плазмы. | | Зеленый, легковоспламеняющийся и [[Врач#Отравление, радиация и другие вредные частицы|радиоактивный]] при вдыхании газ. Горит в присутствии кислорода с выделением огромного (284 кДж/моль) количества тепла. Получается как побочный продукт при горении плазмы. | ||
| 10 | | 10 | ||
| 6 | | 6 | ||
| 2.5 | | 2.5 | ||
| [[Химия#chem_Tritium | Тритий]] | |||
|- | |- | ||
! | ! <center>{{Gas|Frezon}}</center><br>Фрезон | ||
| Синий газ, при вдыхании вызывает галлюцинации и рак. Используется в качестве промышленного хладагента. Некоторые используют его в рекреационных целях из-за его эйфорического эффекта, прежде чем их легкие замерзнут. Самый дорогой и следовательно эффективный для продажи в карго газ. | | Синий газ, при вдыхании вызывает галлюцинации и рак. Используется в качестве промышленного хладагента (при реакции с азотом поглощает 600 кДж/моль). Некоторые используют его в рекреационных целях из-за его эйфорического эффекта, прежде чем их легкие замерзнут. Самый дорогой и следовательно эффективный для продажи в карго газ. | ||
| 600 | | 600 | ||
| 50 | | 50 | ||
| | | 1 | ||
| [[Химия#chem_Frezon | Фрезон]] | |||
|} | |} | ||
<h2 style="border-bottom:2px solid #{{ColorPalette| | <h2 style="border-bottom:2px solid #{{ColorPalette|Atmospheric|Primary Bold}}>Реакции газов</h2> | ||
{| class="wikitable sortable" style="width:100%" | {| class="wikitable sortable" style="width: 100%" | ||
|- | |- | ||
! rowspan="2" style="border-bottom:1px solid gold"| Название | ! rowspan="2" style="border-bottom:1px solid gold"| Название | ||
| Строка 87: | Строка 97: | ||
! rowspan="2" style="border-bottom:1px solid gold"| Продукты | ! rowspan="2" style="border-bottom:1px solid gold"| Продукты | ||
! colspan="2" | Минимальная температура | ! colspan="2" | Минимальная температура | ||
! | ! colspan="2" | Максимальная температура | ||
|- | |- | ||
! style="border-bottom:1px solid gold"| В цельсиях | |||
! style="border-bottom:1px solid gold"| В кельвинах | |||
! style="border-bottom:1px solid gold"| В цельсиях | ! style="border-bottom:1px solid gold"| В цельсиях | ||
! style="border-bottom:1px solid gold"| В кельвинах | ! style="border-bottom:1px solid gold"| В кельвинах | ||
|- | |- | ||
! Горение плазмы | ! Горение плазмы | ||
| Плазма | | Плазма + Кислород | ||
| Углекислый газ | | Углекислый газ + Малое количество трития + Нагрев атмосферы | ||
| 100 | | 100 | ||
| 373.149 | | 373.149 | ||
| | | - | ||
| - | |||
|- | |- | ||
! Горение трития | ! Горение трития | ||
| Тритий + Кислород | | Тритий + Кислород | ||
| Углекислый газ | | Углекислый газ + Водяной пар + Нагрев атмосферы | ||
| 100 | | 100 | ||
| 373.149 | | 373.149 | ||
| | | - | ||
| - | |||
|- | |- | ||
! Производство фрезона | ! Производство фрезона | ||
| Азот + Кислород + Тритий | | Азот + Кислород + Тритий | ||
| Фрезон | | Фрезон + Азот | ||
| - | |||
| - | |||
| -200 | | -200 | ||
| 73.15 | | 73.15 | ||
|- | |- | ||
! Охлаждение фрезона | ! Охлаждение фрезона | ||
| Фрезон + Азот | | Фрезон + Азот | ||
| Охлаждение атмосферы | | Охлаждение атмосферы + Оксид азота | ||
| -250 | | -250 | ||
| 23.15 | | 23.15 | ||
| | | - | ||
| - | |||
|- | |- | ||
! Разложение оксида азота | ! Разложение оксида азота | ||
| Строка 125: | Строка 141: | ||
| 576.85 | | 576.85 | ||
| 850 | | 850 | ||
| | | - | ||
| - | |||
|- | |- | ||
! Реакция миазм с кислородом | ! Реакция миазм с кислородом | ||
| Миазмы + Кислород | | Миазмы + Кислород | ||
| | | Оксид азота + водяной пар | ||
| 50 | | 50 | ||
| 323.149 | | 323.149 | ||
| | | - | ||
| - | |||
|} | |} | ||
<h2 style="border-bottom:2px solid #{{ColorPalette| | ===Реакция горения плазмы=== | ||
Тритий — ценнейший газ, образующийся при сгорании плазмы в условиях перенасыщения кислородом. Он находит основное применение в производстве фрезона и создании бомб, что делает его стратегическим ресурсом для ученых и не только учёных. Контроль уровня кислорода в атмосфере критичен для эффективного синтеза трития, поскольку слишком низкая или высокая концентрация может существенно снизить выход реакции. | |||
Для успешного получения трития недостаточно просто сжечь плазму в кислороде — необходимо создать условия перенасыщения. Это означает, что соотношение кислорода к плазме должно превышать определённый порог, после чего эффективность реакции начинает зависеть от степени перенасыщения. | |||
Перенасыщение вычисляется по следующей формуле: | |||
<div style="border:2px solid black;border-radius:15px;text-align:center;overflow:hidden"><div style="padding-top:3px;padding-bottom:3px;border-bottom:1px solid>Формула перенасыщения</div><div style="color:#fff;padding:5px;font-size:1.1em">перенасыщение = (Моль Кислорода/Моль Плазмы - 32) / 64</div> | |||
<div style="color:#fff;padding:5px;text-align:left;font-size:1.1em"> | |||
где: | |||
* Порог перенасыщения — 96%. | |||
* Порог окончания перенасыщения — порог перенасыщения, делённый на три (32%). | |||
* Разница между этими значениями составляет 64% | |||
</div> | |||
</div> | |||
Это означает, что перенасыщение достигает максимума при концентрации плазмы около 1,538% (приблизительно 20/13). | |||
Перенасыщение в реакции горения плазмы напрямую влияет на эффективность производства трития: если концентрация плазмы близка к 1,538%, выход трития достигает 100%. При более высокой концентрации плазмы реакция перерастает в образование углекислого газа, а при концентрации плазмы выше 3% продуктом реакции становится исключительно углекислый газ. | |||
Тем не менее, перенасыщение само по себе недостаточно — ключевым фактором является температура. Чем выше температура среды, тем быстрее протекает реакция, и тем больше трития образуется. В идеальных условиях, при высоких температурах и достаточном перенасыщении, можно достичь максимального выхода трития. | |||
* При температуре выше 1643,15 K (1370°C) реакция достигает максимальной интенсивности. | |||
* При температуре ниже 373,15 K (100°C) горение прекращается. | |||
[[Файл:TemperatureScale .png|мини|справа|Зависимость выхода трития от температуры]] | |||
Таким образом, для достижения максимального выхода трития атмосферный техник должен создать идеальные условия для реакции: довести атмосферу камеры сгорания до перенасыщения кислородом, а затем нагреть смесь до минимальной температуры. Чем выше температура, тем быстрее процесс получения трития. | |||
[[Файл:PlasmaFireReaction.jpg|центр|альт=Тритий|Установка для создания трития]] | |||
Смесь плазмы и кислорода, которая предварительно подготавливается в смесителе поступает в камеру сгорания. Важно поддерживать правильное соотношение газов, поэтому перед началом работы камеру заполняют смесью 1:99 плазмы и кислорода, а затем, во время работы, поддерживают соотношение 54:46. Сжигание происходит в герметичной камере, где газ нагревается, увеличивая давление. Чтобы предотвратить чрезмерное увеличение давления в камере, система использует радиаторы, охлаждающие газ выходящий из инжектора. Для этого в отдельный замкнутый контур закачивается фрезон, который сначала проходит через камеру, поглощая тепло, а затем охлаждается во внешних радиаторах. Запуск охлаждения осуществляется только при перегреве, чтобы температура держалась на уровне 1643K. Отработанные газы, включая водяной пар и углекислый газ, необходимо регулярно удалять из камеры через систему скрубберов, чтобы избежать неконтролируемого роста давления. Важное отличие от открытых камер заключается в том, что кислород здесь не выбрасывается в космос, а накапливается, поэтому его уровень необходимо контролировать. Если кислорода слишком много, его поступление в смесь снижают, если слишком мало – увеличивают. Для получения начального количества фрезона нужно использовать камеру в открытом виде (для этого она оборудована гермозатвором). Дополнительную подсистему охлаждения инжектора можно не строить и использовать камеру в открытом виде, если эффективность потребления плазмы не важна. | |||
Тритий, пойманный скрубберами, затем фильтруется и может быть направлен в хранилище или использован для дальнейших реакций. | |||
===Производство фрезона=== | |||
Фрезон — это редчайший и один из самых дорогих газов на станции, ценимый за свою уникальную способность охлаждать окружающую среду до экстремальных -250 °C. Однако процесс его добычи крайне сложен: неправильная настройка системы может привести к уничтожению трития. Ошибка в процессе может обернуться большими потерями, поскольку каждая молекула фрезона буквально на вес золота (1 моль фрезона — 1 кредит). | |||
Процесс производства фрезона основан на реакции кислорода и трития с участием азота в качестве катализатора. Однако ключевым фактором, влияющим на выход фрезона, является температура: чем она выше, тем эффективнее идет реакция. Избыточный азот может замедлить процесс и привести к неконтролируемому охлаждению. | |||
Для производства фрезона необходимо соблюсти следующие пропорции: из 1 моля трития и 8 молей кислорода получается соответствующее количество фрезона, умноженное на эффективность реакции. Каждый тик производства приводит к получению 1/50 от этого количества. | |||
Эффективность реакции зависит от температуры: | |||
* При -200 °C процесс идет максимально эффективно. | |||
* При температуре ниже -200 °C эффективность начинает снижаться. | |||
[[Файл:FrezonProductionReaction.png|мини|справа|Зависимость выхода фрезона от температуры]] | |||
Азот играет двойную роль в процессе производства фрезона: он катализирует реакцию, но часть азота остаётся в системе, что может оказать влияние на эффективность процесса. Если температура слишком низкая (около -250 °C), азот начинает взаимодействовать с фрезоном, что дополнительно охлаждает систему и замедляет процесс. Поэтому важно поддерживать правильную концентрацию азота в системе. Если его слишком много, выход фрезона будет снижаться, и в конечном итоге установка может "замерзнуть". | |||
[[Файл:FrezonProduction.png|центр|альт=фрезон|Установка для производства фрезона]] | |||
Тритий поступает в установку прямо из камеры сгорания (зелёная стрелка) или из канистры. Небольшое количество азота можно добавить в установку из газодобытчика или закачать в охладитель перед постройкой (у охладителя есть небольшое внутреннее хранилище). Для стабильной выработки реагенты должны находиться в равных пропорциях, поэтому в установку нужно закачивать кислород по мере необходимости (голубая стрелка). Азот же в свою очередь наоборот будет производиться в процессе реакции и его нужно периодически уничтожать (красная стрелка). Газ в установке должен прокачиваться через несколько фильтров: один фильтрует азот, он не должен блокировать прохождение газа, потому что фильтр не будет включаться часто, другие два постоянно прокачивают смесь через себя и фильтруют холодный оксид азота (фиолетовая стрелка) и желанный фрезон (синяя стрелка). | |||
===Как получить максимум фрезона?=== | |||
* Поддерживайте температуру около -200 °C, чтобы предотвратить переохлаждение установки. | |||
* Контролируйте концентрацию азота: он необходим для реакции, но его избыток может вызвать проблемы при температуре -250 °C. Уничтожайте излишки азота. | |||
* Используйте уже нагретый кислород из камеры сгорания: он быстрее нагреет установку, чем кислород из газодобытчика. | |||
<h2 style="border-bottom:2px solid #{{ColorPalette|Atmospheric|Primary Bold}}>Настройка атмоса</h2> | |||
Атмосферика, иногда называемая Атмосией, - это место, где находится большая часть оборудования для обработки воздуха. Каждая станция имеет различную схему этого отдела. Опытные атмосферные специалисты запоминают атмосферные макеты, потому как частые бесполезные инженерные изменения на станциях при реконструкции могут затруднить работу. | Атмосферика, иногда называемая Атмосией, - это место, где находится большая часть оборудования для обработки воздуха. Каждая станция имеет различную схему этого отдела. Опытные атмосферные специалисты запоминают атмосферные макеты, потому как частые бесполезные инженерные изменения на станциях при реконструкции могут затруднить работу. | ||
===Дистрибутив=== | ===Дистрибутив=== | ||
Главный воздухораспределительный контур станции, также известный как «дистро», снабжает вентиляционные отверстия, которые поставляют воздух в станцию. Обычно он окрашен в тёмно-синий цвет, чтобы его было легко идентифицировать. | Главный воздухораспределительный контур станции, также известный как «дистро», снабжает вентиляционные отверстия, которые поставляют воздух в станцию. Обычно он окрашен в тёмно-синий цвет, чтобы его было легко идентифицировать. | ||
Текущая версия от 19:48, 17 марта 2025
Газы
Тут описаны свойства газов которые есть в SS14 на данный момент
| Газ | Описание | Удельная теплоемкость Дж/(кг·К) | Молярная масса (г/моль) | Цена за Моль (Кредиты) | Конденсируется |
|---|---|---|---|---|---|
 Кислород |
Бесцветный газ без запаха. Люди должны дышать, чтобы оставаться в живых. Окислитель в большинстве реакций горения. | 20 | 32 | 0 | Кислород |
 Азот |
Бесцветный газ без запаха. Сам по себе безопасен при вдыхании человеком. Необходим бля дыхания слаймолюдам и воксам. | 30 | 28 | 0 | Азот |
 Углекислый газ |
Бесцветный газ без запаха. Выдыхается существами, дышащими кислородом. При высокой концентрации он становится токсичным для всех кроме дион. | 30 | 44 | 0 | Диоксид углерода |
 Оксид азота |
Бесцветный газ без запаха. Также известный как «веселящий» или «сонный» газ, он действует как успокаивающее средство на всех, кроме слизней, и токсичен в очень высоких концентрациях. Это вещество выдыхается слизнями. | 40 | 44 | 1 | - |
 
Плазма |
Розово-фиолетовый, легковоспламеняющийся, ядовитый газ. В присутствии кислорода загорается при воспламенители или температуре выше 100 °С. Этот газ жизненно важен для производственной и научной деятельности на борту станции. | 200 | 120 | 0 | Плазма |
 
Водяной пар |
Выглядит как белое облако, вода в газообразном состоянии. Не конденсируется в жидкую воду. Вреден для слаймолюдов. | 40 | 18 | 0 | Вода |
 
Миазмы (Аммиак) |
Тёмно-фиолетовый, зловонный газ. Ядовит и вреден в достаточно больших концентрациях. Побочный продукт неприятных биологических процессов, например, гниения тел. Может выделятся крысиным королём. | 20 | 44 | 0.15 | Аммиак |
 
Тритий |
Зеленый, легковоспламеняющийся и радиоактивный при вдыхании газ. Горит в присутствии кислорода с выделением огромного (284 кДж/моль) количества тепла. Получается как побочный продукт при горении плазмы. | 10 | 6 | 2.5 | Тритий |
 
Фрезон |
Синий газ, при вдыхании вызывает галлюцинации и рак. Используется в качестве промышленного хладагента (при реакции с азотом поглощает 600 кДж/моль). Некоторые используют его в рекреационных целях из-за его эйфорического эффекта, прежде чем их легкие замерзнут. Самый дорогой и следовательно эффективный для продажи в карго газ. | 600 | 50 | 1 | Фрезон |
Реакции газов
| Название | Вещества вступавшие в реакцию | Продукты | Минимальная температура | Максимальная температура | ||
|---|---|---|---|---|---|---|
| В цельсиях | В кельвинах | В цельсиях | В кельвинах | |||
| Горение плазмы | Плазма + Кислород | Углекислый газ + Малое количество трития + Нагрев атмосферы | 100 | 373.149 | - | - |
| Горение трития | Тритий + Кислород | Углекислый газ + Водяной пар + Нагрев атмосферы | 100 | 373.149 | - | - |
| Производство фрезона | Азот + Кислород + Тритий | Фрезон + Азот | - | - | -200 | 73.15 |
| Охлаждение фрезона | Фрезон + Азот | Охлаждение атмосферы + Оксид азота | -250 | 23.15 | - | - |
| Разложение оксида азота | Оксид азота | Азот + Кислород | 576.85 | 850 | - | - |
| Реакция миазм с кислородом | Миазмы + Кислород | Оксид азота + водяной пар | 50 | 323.149 | - | - |
Реакция горения плазмы
Тритий — ценнейший газ, образующийся при сгорании плазмы в условиях перенасыщения кислородом. Он находит основное применение в производстве фрезона и создании бомб, что делает его стратегическим ресурсом для ученых и не только учёных. Контроль уровня кислорода в атмосфере критичен для эффективного синтеза трития, поскольку слишком низкая или высокая концентрация может существенно снизить выход реакции.
Для успешного получения трития недостаточно просто сжечь плазму в кислороде — необходимо создать условия перенасыщения. Это означает, что соотношение кислорода к плазме должно превышать определённый порог, после чего эффективность реакции начинает зависеть от степени перенасыщения.
Перенасыщение вычисляется по следующей формуле:
Это означает, что перенасыщение достигает максимума при концентрации плазмы около 1,538% (приблизительно 20/13).
Перенасыщение в реакции горения плазмы напрямую влияет на эффективность производства трития: если концентрация плазмы близка к 1,538%, выход трития достигает 100%. При более высокой концентрации плазмы реакция перерастает в образование углекислого газа, а при концентрации плазмы выше 3% продуктом реакции становится исключительно углекислый газ.
Тем не менее, перенасыщение само по себе недостаточно — ключевым фактором является температура. Чем выше температура среды, тем быстрее протекает реакция, и тем больше трития образуется. В идеальных условиях, при высоких температурах и достаточном перенасыщении, можно достичь максимального выхода трития.
- При температуре выше 1643,15 K (1370°C) реакция достигает максимальной интенсивности.
- При температуре ниже 373,15 K (100°C) горение прекращается.

Таким образом, для достижения максимального выхода трития атмосферный техник должен создать идеальные условия для реакции: довести атмосферу камеры сгорания до перенасыщения кислородом, а затем нагреть смесь до минимальной температуры. Чем выше температура, тем быстрее процесс получения трития.

Смесь плазмы и кислорода, которая предварительно подготавливается в смесителе поступает в камеру сгорания. Важно поддерживать правильное соотношение газов, поэтому перед началом работы камеру заполняют смесью 1:99 плазмы и кислорода, а затем, во время работы, поддерживают соотношение 54:46. Сжигание происходит в герметичной камере, где газ нагревается, увеличивая давление. Чтобы предотвратить чрезмерное увеличение давления в камере, система использует радиаторы, охлаждающие газ выходящий из инжектора. Для этого в отдельный замкнутый контур закачивается фрезон, который сначала проходит через камеру, поглощая тепло, а затем охлаждается во внешних радиаторах. Запуск охлаждения осуществляется только при перегреве, чтобы температура держалась на уровне 1643K. Отработанные газы, включая водяной пар и углекислый газ, необходимо регулярно удалять из камеры через систему скрубберов, чтобы избежать неконтролируемого роста давления. Важное отличие от открытых камер заключается в том, что кислород здесь не выбрасывается в космос, а накапливается, поэтому его уровень необходимо контролировать. Если кислорода слишком много, его поступление в смесь снижают, если слишком мало – увеличивают. Для получения начального количества фрезона нужно использовать камеру в открытом виде (для этого она оборудована гермозатвором). Дополнительную подсистему охлаждения инжектора можно не строить и использовать камеру в открытом виде, если эффективность потребления плазмы не важна.
Тритий, пойманный скрубберами, затем фильтруется и может быть направлен в хранилище или использован для дальнейших реакций.
Производство фрезона
Фрезон — это редчайший и один из самых дорогих газов на станции, ценимый за свою уникальную способность охлаждать окружающую среду до экстремальных -250 °C. Однако процесс его добычи крайне сложен: неправильная настройка системы может привести к уничтожению трития. Ошибка в процессе может обернуться большими потерями, поскольку каждая молекула фрезона буквально на вес золота (1 моль фрезона — 1 кредит).
Процесс производства фрезона основан на реакции кислорода и трития с участием азота в качестве катализатора. Однако ключевым фактором, влияющим на выход фрезона, является температура: чем она выше, тем эффективнее идет реакция. Избыточный азот может замедлить процесс и привести к неконтролируемому охлаждению.
Для производства фрезона необходимо соблюсти следующие пропорции: из 1 моля трития и 8 молей кислорода получается соответствующее количество фрезона, умноженное на эффективность реакции. Каждый тик производства приводит к получению 1/50 от этого количества.
Эффективность реакции зависит от температуры:
- При -200 °C процесс идет максимально эффективно.
- При температуре ниже -200 °C эффективность начинает снижаться.
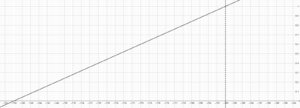
Азот играет двойную роль в процессе производства фрезона: он катализирует реакцию, но часть азота остаётся в системе, что может оказать влияние на эффективность процесса. Если температура слишком низкая (около -250 °C), азот начинает взаимодействовать с фрезоном, что дополнительно охлаждает систему и замедляет процесс. Поэтому важно поддерживать правильную концентрацию азота в системе. Если его слишком много, выход фрезона будет снижаться, и в конечном итоге установка может "замерзнуть".

Тритий поступает в установку прямо из камеры сгорания (зелёная стрелка) или из канистры. Небольшое количество азота можно добавить в установку из газодобытчика или закачать в охладитель перед постройкой (у охладителя есть небольшое внутреннее хранилище). Для стабильной выработки реагенты должны находиться в равных пропорциях, поэтому в установку нужно закачивать кислород по мере необходимости (голубая стрелка). Азот же в свою очередь наоборот будет производиться в процессе реакции и его нужно периодически уничтожать (красная стрелка). Газ в установке должен прокачиваться через несколько фильтров: один фильтрует азот, он не должен блокировать прохождение газа, потому что фильтр не будет включаться часто, другие два постоянно прокачивают смесь через себя и фильтруют холодный оксид азота (фиолетовая стрелка) и желанный фрезон (синяя стрелка).
Как получить максимум фрезона?
- Поддерживайте температуру около -200 °C, чтобы предотвратить переохлаждение установки.
- Контролируйте концентрацию азота: он необходим для реакции, но его избыток может вызвать проблемы при температуре -250 °C. Уничтожайте излишки азота.
- Используйте уже нагретый кислород из камеры сгорания: он быстрее нагреет установку, чем кислород из газодобытчика.
Настройка атмоса
Атмосферика, иногда называемая Атмосией, - это место, где находится большая часть оборудования для обработки воздуха. Каждая станция имеет различную схему этого отдела. Опытные атмосферные специалисты запоминают атмосферные макеты, потому как частые бесполезные инженерные изменения на станциях при реконструкции могут затруднить работу.
Дистрибутив
Главный воздухораспределительный контур станции, также известный как «дистро», снабжает вентиляционные отверстия, которые поставляют воздух в станцию. Обычно он окрашен в тёмно-синий цвет, чтобы его было легко идентифицировать.
Отходы
Отходы обычно отмечены красными трубами и отвечают за удаление отработанного газа вокруг станции через скрубберы. Эти трубы начинаются и заканчиваются в атмосе и огибают всю станцию. Основное назначение системы отходов – обеспечить удаление вредных газов из атмосферы станции. Скрубберы удалят газ из коридоров и вернут его в атмос, где он будет разделен газовыми фильтрами на различные камеры хранения. Вредные газы будут оседать в предназначенных для них камерах, а пригодный для дыхания воздух снова вернется в дистро и на станцию, чтобы продолжить цикл.
Камера смешивания
Камера смешивания представляет собой пустую зону хранения с собственной отдельной петлёй труб и насосов в атмосфере. Смесительная петля обычно отмечена коричневыми трубами, а камера хранения обычно находится рядом с внешним корпусом, отделённая от станции усиленными стенами и окнами. Рядом будет аварийная кнопка, чтобы разгерметизировать камеру, если вам нужно сбросить смесь в случае аварии или вы просто хотите опустошить камеру для новой смеси. Камера смешивания предназначена для экспериментов с различными смесями, соотношениями, температурами и давлениями при комбинировании газов.